UP Board Solutions for Class 11 Chemistry Chapter 8 Redox Reactions (अपचयोपचय अभिक्रियाएँ)
These Solutions are part of UP Board Solutions for Class 11 Chemistry. Here we have given UP Board Solutions for Class 11 Chemistry Chapter 8 Redox Reactions (अपचयोपचय अभिक्रियाएँ).
पाठ के अन्तर्गत दिए गए प्रश्नोत्तर
प्रश्न 1.
निम्नलिखित स्पीशीज में प्रत्येक रेखांकित तत्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
(क) NaH2PO4
(ख) Na HSO4
(ग) H4P2O7
(घ) K2MnO4
(ङ) CaO2
(च) NaBH4
(छ) H2S2O7
(ज) KAl(SO4).12H2O
उत्तर



प्रश्न 2.
निम्नलिखित यौगिकों के रेखांकित तत्वों की ऑक्सीकरण संख्या क्या है तथा इन परिणामों को आप कैसे प्राप्त करते हैं?
(क) KI3
(ख) H2S4O6
(ग) Fe3O4
(घ) CH2CH2OH
(ङ) CH3COOH
उत्तर




प्रश्न 3.
निम्नलिखित अभिक्रियाओं का अपचयोपचय अभिक्रियाओं के रूप में औचित्य स्थापित करने का प्रयास कीजिए–
(क) CuO(s)+ H2(g) + Cu(s) + H2O(g)
(ख) Fe2O3(s) + 3CO(g)—-→ 2Fe(s) + 3CO2(g)
(ग) 4BCl3(g) + 3LiAlH4(s) → 2B2H6(g) + 3LiCl(s) + 3AlCl3(s)
(घ) 2K(s) + F2(g) → 2K+F– (s)
(ङ) 4NH3(g) + 5O2(g) → 4NO(g) + 6H2O(g)
उत्तर
![]()
इस अभिक्रिया में, Cu की ऑक्सीकरण अवस्था +2(CuO में) से घटकर शून्य (Cu में) हो जाती है जबकि H की ऑक्सीकरण अवस्था शून्य (H2 में) से बढ़कर +1(H2O में) हो जाती है। इसलिए अभिक्रिया में CuO का अपचयन तथा H का ऑक्सीकरण हो रहा है। अतः यह एक अपचयोपचय अभिक्रिया है।
![]()
इस अभिक्रिया में, Fe2O3 का अपचयन हो रहा है क्योंकि Fe की ऑक्सीकरण अवस्था +3(Fe2O3 में) से घटकर शून्य (Fe में) हो जाती है। CO का ऑक्सीकरण हो रहा है क्योंकि C की ऑक्सीकरण अवस्था +2 (CO में) से बढ़कर +4 (CO,2में) हो जाती है। अत: यह एक अपचयोपचय अभिक्रिया (redox reaction) है।
![]()
इस अभिक्रिया में, BCl3 का अपचयन हो रहा है क्योकि B की ऑक्सीकरण अवस्था +3 (BCl3 में) से घटकर -3 (B2H6 में) हो जाती है तथा LiAlH4 का ऑक्सीकरण हो रहा है क्योकि H की ऑक्सीकरण अवस्था -1(LiAlH4 में) से बढ़कर +1 (B2H6 में) हो जाती है। अतः यह एक अपचयोपचय (redox) अभिक्रिया है।
![]()
इस अभिक्रिया में, K का ऑक्सीकरण हो रहा है क्योंकि इसकी ऑक्सीकरण अवस्था शून्य से बढ़कर +1 हो जाती है तथा F को अपचयन हो रहा है क्योंकि इसकी ऑक्सीकरण अवस्था । शून्य से घटकर -1 हो जाती है। अत: यह एक अपचयोपचय अभिक्रिया है।
![]()
इस अभिक्रिया में, NH3 को ऑक्सीकरण हो रहा है क्योंकि इसकी ऑक्सीकरण अवस्था -3 से बढ़कर +2 हो जाती है तथा O2 का अपचयन हो रहा है क्योंकि इसकी ऑक्सीकरण अवस्था शून्य से घटकर -2 (H2O में) हो जाती है। अतः यह एक अपचयोपचय (redox) अभिक्रिया है।
प्रश्न 4.
फ्लुओरीन बर्फ से अभिक्रिया करके यह परिवर्तन लाती है
H2O(s) + F2(g) → HF(g) + HOF(g)
इस अभिक्रिया का अपचयोपचय औचित्य स्थापित कीजिए।
उत्तर
H2O(s) + F (g) → HF(g) + HOF (g)
इस अभिक्रिया में, F2 का अपचयन के साथ-साथ ऑक्सीकरण भी हो रहा है क्योंकि यह H (वैद्युत धनात्मक तत्त्व) को जोड़कर HF बनाती है तथा 0 (एक वैद्युत ऋणात्मक तत्त्व) को जोड़कर HOF बनाती है। अत: यह एक ऑक्सीकरण अपचयन अभिक्रिया (redox reaction) है।
प्रश्न 5.
H2SO5, Cr2O2-7 तथा NO–3 में सल्फर, क्रोमियम तथा नाइट्रोजन की ऑक्सीकरण संख्या की गणना कीजिए। साथ ही इन यौगिकों की संरचना बताइए तथा इसमें हेत्वाभास | (fallacy) का स्पष्टीकरण दीजिए।
उत्तर
(i) H2SO5 में S की ऑक्सीकरण संख्या :
(+1)x2 + (x) + [(-2)x5]= 0
अथवा x= 10-2= +8
S की ऑक्सीकरण संख्या +8 सम्भव नहीं है क्योंकि s के बाह्य कोश में 6 इलेक्ट्रॉन होते हैं और उसकी अधिकतम ऑक्सीकरण संख्या +6 हो सकती है। अत: H, SO में दो ऑक्सीकरण परमाणुओं को एक-दूसरे से जुड़ा होना चाहिए। इस हेत्वाभास (fallacy) को H2SO4 की निम्नलिखित संरचना द्वारा स्पष्ट किया जा सकता है

(ii) Cr2O2-7 में Cr की ऑक्सीकरण संख्या :

(iii) NO–3 में N की ऑक्सीकरण संख्या :


प्रश्न 6.
निम्नलिखित यौगिकों के सूत्र लिखिए-
(क) मर्करी (II) क्लोराइड
(ख) निकिल (II) सल्फेट
(ग) टिन (IV) ऑक्साइड
(घ) थैलियम (I) सल्फेट
(ङ) आयरन (II) सल्फेट
(च) क्रोमियम (III) ऑक्साइड
उत्तर
(क) HgCl2
(ख) NiSO4
(ग) SnO2
(घ) Th2SO4
(ङ) Fe2(SO4 )3
(च) Cr2O7
प्रश्न 7.
उन पदार्थों की सूची तैयार कीजिए जिनमें कार्बन-4 से +4 तक की तथा नाइट्रोजन-3 से +5 तक की ऑक्सीकरण अवस्था होती है।
उत्तर

प्रश्न 8.
अपनी अभिक्रियाओं में सल्फर डाइऑक्साइड तथा हाइड्रोजन परॉक्साइड ऑक्सीकारक तथा अपचायक-दोनों ही रूपों में क्रिया करते हैं, जबकि ओजोन तथा नाइट्रिक अम्ल केवल ऑक्सीकारक के रूप में ही। क्यों?
उत्तर
SO2 में S की ऑक्सीकरण संख्या +4 होती है। S अपनी अभिक्रियाओं में -2 और +6 के बीच की कोई भी ऑक्सीकरण-संख्या दर्शा सकता है। अत: SO2 में S की ऑक्सीकरण संख्या घट सकती है और बढ़ भी सकती है; अर्थात् इसका ऑक्सीकरण तथा अपचयन दोनों सम्भव है। इस कारण SO2 ऑक्सीकारक तथा अपचायक दोनों अभिकर्मकों की तरह व्यवहार करती है। H2O2 की स्थिति भी समान प्रकार की है। H2O2 में, O की ऑक्सीकरण अवस्था -1 होती है। ऑक्सीजन -2 और 0 (शून्य) के बीच की कोई भी ऑक्सीकरण अवस्था दर्शाता है (+2 भी जब F से जुड़ा होता है) अतः H2O2 में ऑक्सीजन अपनी ऑक्सीकरण संख्या घटा तथा बढ़ा सकता है। इस कारण H2O2 ऑक्सीकारक तथा अपचायक दोनों अभिकर्मकों की तरह व्यवहार करता है।
O3 में, ऑक्सीजन की ऑक्सीकरण अवस्था शून्य है। यह अपनी ऑक्सीकरण-अवस्था को -1 तथा -2 तक घटा सकता है परन्तु अपनी ऑक्सीकरण-अवस्था को बढ़ा नहीं सकता। अत: O3 केवल एक ऑक्सीकारक की तरह व्यवहार करती है। H2O2 की स्थिति भी समान प्रकार की है। HNO3 में, N की ऑक्सीकरण-अवस्था +5 होती है जो N की अधिकतम ऑक्सीकरण अवस्था है। अत: N केवल अपनी ऑक्सीकरण अवस्था घटा सकता है। इस कारण HNO3 केवल ऑक्सीकारक की तरह व्यवहार करता है।
प्रश्न 9.
इन अभिक्रियाओं को देखिए
(क) 6CO2(g) + 6H2O(l) → C6H12O6 (aq) + 6O2(g)
(ख) O3(g) + H2O2(l) → H2O(l) + 2O2(g)
बताइए कि इन्हें निम्नलिखित ढंग से लिखना ज्यादा उचित क्यों है?
(क) 6CO2(g) + 12H2O(I) → C2H12O6 (aq) + 6H2O(I) + 6O2(g)
(ख) O2(g) + H2O2(l) → H2O(I) + O2(g) + O2(g)
उपर्युक्त अपचयोपचय अभिक्रियाओं (क) तथा (ख) के अन्वेषण की विधि सुझाइए।
उत्तर
(क) यह प्रकाश संश्लेषण (photosynthesis) की अभिक्रिया है जो कि एक बहुत ही जटिल प्रक्रिया है और अनेक चरणों में सम्पन्न होती है। इस अभिक्रिया में, 12H2O अणु क्लोरोफिल (chlorophyll) की उपस्थिति में पहले अपघटित होकर H2 तथा O2 देते हैं। इस प्रकार निर्मित H2CO2 को अपचयित कर C2H12O6 का निर्माण करती है। अतः अभिक्रिया को एक सरल रूप में अभिक्रिया निम्न प्रकार दिखाया जा सकता है|

इसलिए इस अभिक्रिया को समीकरण (iii) की भाँति लिखना ज्यादा उचित है। इस निरूपण में 12H2O अणु भाग लेते हैं तथा 6H2O अणु उत्पन्न होते हैं।
(ख) दी गई अभिक्रिया का वास्तविक प्रारूप निम्न प्रकार है-

समीकरण (iii) प्रदर्शित करती है कि O2 का एक अणु O3 से प्राप्त होता है, जबकि दूसरा H2O2 से प्राप्त होता है। इसलिए, समीकरण को प्रदर्शित करने की यह विधि अधिक उपयुक्त है। समीकरण (क) तथा (ख) का अन्वेषण ट्रेसर तकनीक (tracer technique) के द्वारा किया जा सकता है। समीकरण (क) में H2O18 तथा समीकरण (ख) में H2O18 (या O183) का प्रयोग कर अभिक्रिया के पथ को निर्धारित किया जा सकता है।
प्रश्न 10.
AgF2 एक अस्थिर यौगिक है। यदि यह बन जाए तो यह यौगिक एक अति शक्तिशाली ऑक्सीकारक की भाँति कार्य करता है। क्यों?
उत्तर
AgF2 में, Ag की ऑक्सीकरण-अवस्था +2 होती है जो Ag की अत्यधिक अस्थायी अवस्था है। इसलिए, यह एक इलेक्ट्रॉन ग्रहण करने के बाद शीघ्रता से अपचयित होकर स्थायी ऑक्सीकरण-अवस्था +1 प्राप्त कर लेता है।

इसी कारण AgF2 (यदि प्राप्त हो जाये) एक अत्यन्त प्रबल ऑक्सीकारक की भाँति व्यवहार करता है।
प्रश्न 11.
“जब भी एक ऑक्सीकारक तथा अपचायक के बीच अभिक्रिया सम्पन्न की जाती है, तब अपंचायक के आधिक्य में निम्नतर ऑक्सीकरण अवस्था का यौगिक तथा ऑक्सीकारक के आधिक्य में उच्चतर ऑक्सीकरण अवस्था का यौगिक बनता है। इस वक्तव्य का औचित्य तीन उदाहरण देकर दीजिए।
उत्तर
दिये गये वक्तव्य का औचित्य निम्नलिखित उदाहरणों द्वारा स्पष्ट किया जा सकता है

अभिक्रिया (i) में अपचायक (reducing agent) कार्बन अधिकता में है, जबकि अभिक्रिया (ii) में ऑक्सीकारक (oxidising agent) O2 अधिकता में है। अभिक्रिया (i) में CO (कार्बन की O.S.= +2) तथा अभिक्रिया (ii) में CO2 (कार्बन की O.S. = +4) का निर्माण होता है।

प्रश्न 12.
इन प्रेक्षणों की अनुकूलता को कैसे समझाएँगे?
(क) यद्यपि क्षारीय पोटैशियम परमैंगनेट तथा अम्लीय पोटैशियम परमैंगनेट दोनों ही
ऑक्सीकारक हैं। फिर भी टॉलूईन से बेन्जोइक अम्ल बनाने के लिए हम ऐल्कोहॉलिक पोटैशियम परमैंगनेट का प्रयोग ऑक्सीकारक के रूप में क्यों करते हैं? इस अभिक्रिया के लिए सन्तुलित अपचयोपचय समीकरण दीजिए।
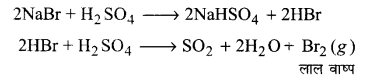
(ख) क्लोराइडयुक्त अकार्बनिक यौगिक में सान्द्र सल्फ्यूरिक अम्ल डालने पर हमें तीक्ष्ण गन्ध वाली HCI गैस प्राप्त होती है, परन्तु यदि मिश्रण में ब्रोमाइड उपस्थित हो तो हमें ब्रोमीन की लाल वाष्प प्राप्त होती है, क्यों?
उत्तर
(क) यदि टॉलूईन का ऑक्सीकरण क्षारीय अथवा अम्लीय KMnO4 द्वारा किया जाये तो ऑक्सीकरण को नियन्त्रित करना कठिन होगा। इसमें मुख्य उत्पाद बेंजोइक ऐसिड (benzoic acid) के साथ-साथ सह अभिक्रियाओं (side reactions) द्वारा दूसरे उत्पाद भी प्राप्त होंगे। इसलिए टॉलूईन के ऑक्सीकरण के लिये क्षारीय अथवा अम्लीय KMnO4 के स्थान पर ऐल्कोहॉलिक KMnO4 को वरीयता दी जाती है। अपचयोपचय (redox reaction) अभिक्रिया नीचे दी गई है–


(ख) जब सान्द्र H2SO4 को क्लोराइडयुक्त एक अकार्बनिक मिश्रण में मिलाया जाता है, तो कम वाष्पशील अम्ल H2SO4 अधिक वाष्पशील अम्ल HCl को विस्थापित करता है और HCl गैस की तीक्ष्ण गन्ध आती है।
2NaCl (5) + H2SO4 (l) → 2NaHSO4 (s) + 2HCl(g)
HCl एक दुर्बल अपचायक है। यह H2SO4 को SO2 में अपचयित करने में असमर्थ है। जब मिश्रण में ब्रोमाइड उपस्थित होता है तो अधिक उड़नशील अम्ल HBr विस्थापित होता है। HBr एक अधिक प्रबल अपचायक है और H2SO4 को SO2 में अपचयित कर देता है। यह स्वयं ऑक्सीकृत होकर ब्रोमीन देता है जो लाल वाष्प के रूप में प्राप्त होती है।
प्रश्न 13.
निम्नलिखित अभिक्रियाओं में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए-
(क) 2AgBr(s) + C6H6O2(aq) → 2Ag(s) + 2HBr (aq) + C6H4O2(aq)
(ख) HCHO(7) +2[Ag(NH3)2]+ (aq) + 3OH– (aq) → 2Ag(s)+ HCOO–7 (aq) +4NH3(aq) +2H2O(7)
(ग) HCHO(1) + 2Cu2+(aq) + 5OH– (aq) → Cu2O(s)+ HCOO– (aq) +3H2O(l)
(घ) N2H4(l) + 2H2O(l) → N2(g)+ 4H2O(l)
(ङ) Pb(s) + PbO2(s)+ 2HSO4 (aq) → 2PbSO4(s) + 2H2O(l)
उत्तर

प्रश्न 14.
निम्नलिखित अभिक्रियाओं में एक ही अपचायक थायोसल्फेट, आयोडीन तथा ब्रोमीन से अलग-अलग प्रकार से अभिक्रिया क्यों करता है?
2S2O2-3 (aq) + I2(s) → S4O2-6(aq) + 2I– (aq)
S2O2-3 (aq) + 2Br2(l) + 5H2O(l) → 2SO2-4 (aq) + 4Br–(aq) + 10H+ (aq)
उत्तर
प्रस्तुत स्पीशीज (species) में S की ऑक्सीकरण संख्या निम्न है-
S2O2-3 = +2, S4O2-6 = 2.5, SO2-4 = +6
ब्रोमीन, आयोडीन से अधिक प्रबल ऑक्सीकारक है। इसलिये यह S2O2-3 (S की 0.S. = +2) को SO2-4 (S की O.S. = +6) में ऑक्सीकृत कर देता है; जिसमें S उच्च-ऑक्सीकरण अवस्था में है। I2 एक दुर्बल ऑक्सीकारक की तरह व्यवहार करता है। यह S2O2-3 को S4O2-6(S की O.S. = 2.5) में . ऑक्सीकृत करता है, जिसमें S की ऑक्सीकरण-अवस्था कम है। यही कारण है कि S2O2-3, Br2 से I2 से अलग-अलग प्रकार से अभिक्रिया करता है।
प्रश्न 15.
अभिक्रिया देते हुए सिद्ध कीजिए कि हैलोजनों में फ्लुओरीन श्रेष्ठ ऑक्सीकारक तथा हाइड्रोहैलिक यौगिकों में हाइड्रोआयोडिक अम्ल श्रेष्ठ अपचायक है।
उत्तर
हैलोजनों की ऑक्सीकारक क्षमता का घटता हुआ क्रम निम्न है-F2 > Cl2, > Br2 > I2। F2 एक प्रबल ऑक्सीकारक है तथा यह Cl–, Br– तथा I– आयनों का ऑक्सीकर कर देती है। Cl2 केवल Br– तथा I– आयनों को और Br2 केवल I– आयनों को ही ऑक्सीकृत कर पाती है। I2 इनमें से किसी को भी ऑक्सीकृत करने में असमर्थ है। अभिक्रियायें नीचे दी गई हैं-
F2 की ऑक्सीकारक अभिक्रियाएँ-
F2(g) + 2Cl–(aq) -→ 2F– (aq) + Cl2 (g)
F2 (g)+2Br–(aq) 2F–(aq) + Br2 (1)
F2(g) + 2I–(aq) → 2F–(aq) + I(s)
Cl2 की ऑक्सीकारक अभिक्रियाएँ-
Cl2(g)+ 2Br–(aq) -→ 2Cl–(aq) + Br (1)
Cl2(g) + 2I–(aq) → 2C–(aq) + I2(l),
I2 की ऑक्सीकारक अभिक्रियाएँ-
Br2(l) + 2I–(aq) → 2Br–(aq) + I2(s)
इस प्रकार F2 सबसे अच्छा ऑक्सीकारक है। हाइड्रोलिक अम्लों की अपचायक क्षमता का घटता हुआ क्रम निम्न प्रकार है-
HI> HBr> HCl> HF
HI और HBr सल्फ्यूरिक अम्ल (H2SO4) को SO2 में अपचयित कर देते हैं, जबकि HCl व HF ऐसा नहीं कर पाते।
2HBr + H2SO4 → SO2+ 2H2O+ Br2
2HI + H2SO4 → SO2 + 2H2O + I2
HCI, MnO2 को Mn2+ में अपचयित कर देता है परन्तु HF ऐसा करने में असमर्थ है। यह दर्शाता है। कि HCl की ऑक्सीकृत क्षमता HBr से अधिक है।
MnO2 +4HCl → MnCl2 + Cl2 + 2H2O
MnO2 + 4HF → कोई अभिक्रिया नहीं
अतः हाइड्रोलिक अम्लों में HI प्रबलतम अपचायक है।
प्रश्न 16.
निम्नलिखित अभिक्रिया क्यों होती है?
XeO4-6(aq) + 2F–(aq) + 6H+(aq) → XeO3(g) + F2(g) + 3H2O(I)
यौगिक Na4XeO6 (जिसका एक भाग XeO4-6 है) के बारे में आप इस अभिक्रिया में क्या निष्कर्ष निकाल सकते हैं?
उत्तर
![]()
इस अभिक्रिया में XeO6 को XeO3 में अपचयन तथा F– का F2 में ऑक्सीकरण हो रहा है। यह अभिक्रिया इसलिये सम्पन्न होती है क्योंकि XeO6, F2 से अधिक प्रबल ऑक्सीकारक है। चूंकि XeO4-6 F2 की तुलना में अधिक प्रबल ऑक्सीकारक है, अत: Na4XeO6 एक प्रबल ऑक्सीकारक होगा।
प्रश्न 17.
निम्नलिखित अभिक्रियाओं में-
(क) H3PO2(aq) + 4AgNO3(aq) + 2H2O(l) → H2PO4(aq) + 4Ag(s) +4HNO3(aq)
(ख) H3PO2(aq) + 2CuSO4 (aq) + 2H2O(I)→ H3PO4 (aq) + 2Cu(s) +2H2SO4 (aq)
(ग) C2H5CHO(l) + 2[Ag(NH3)2]+(aq) + 3OH– (aq) → C6H5COO– (aq) +2Ag(s) +4NH3(aq) +2H2O(l)
(घ) C6H5CHO(l) +2Cu2+ (aq) + 5OH– (aq) कोई परिवर्तन नहीं।
इन अभिक्रियाओं से A+ तथा Cu2+ के व्यवहार के विषय में निष्कर्ष निकालिए।
उत्तर
ये अभिक्रिया दर्शाती है कि Ag+,Cu2+ से अधिक प्रबल ऑक्सीकारक है। यह निम्न तथ्यों से स्पष्ट है-
- अभिक्रिया (क) और (ख) दर्शाती है कि Ag2व Cu2+ दोनों आयने H3PO2 को H3PO4 में ऑक्सीकृत कर सकते हैं। अत: दोनों ऑक्सीकारक हैं।।
- अभिक्रिया (ग) दर्शाती है कि [Ag(NH3)2]+ आयन C6H5CHO को C6H2COOH में ऑक्सीकृत कर सकता है, परन्तु अभिक्रिया (घ) के अनुसार Cu2+ आयन ऐसा करने में असमर्थ है।
अतः यह निष्कर्ष निकाला जा सकता है कि यद्यपि Ag+व Cu2+ दोनों ऑक्सीकारक अभिकर्मक हैं, परन्तु Ag+,Cu2+ से अधिक प्रबल ऑक्सीकारक है।
प्रश्न 18.
आयन-इलेक्ट्रॉन विधि द्वारा निम्नलिखित रेडॉक्स अभिक्रियाओं को सन्तुलित कीजिए-
(क) MnO–4(aq) +I–(aq) → MnO2(s) +I2(s)
(क्षारीय माध्यम)
(ख) MnO–4(aq) + SO2(8) → Mn2+ (aq) + HSO–4(aq) (अम्लीय माध्यम)
(ग) H2O2(aq) +Fe2+ (aq) → Fe3+ (aq) +H2O(l) (अम्लीय माध्यम)
(घ) Cr2O2-7 +SO2(g) → Cr3+ (aq) + SO2-4(aq) (अम्लीय माध्यम)
उत्तर






प्रश्न 19.
निम्नलिखित अभिक्रियाओं के समीकरणों को आयन-इलेक्ट्रॉन तथा ऑक्सीकरण संख्या विधि (क्षारीय माध्यम में) द्वारा सन्तुलित कीजिए तथा इनमें ऑक्सीकारक और
अपचायकों की पहचान कीजिए-
(क) P4(s) + OH– (aq) → PH3(g) + H–PO27 (aq)
(ख) N2H4(l) + ClO–3(aq) → NO(g) + Cl–(g)
(ग) Cl2O7(g) + H2O2(aq) → ClO–2 (aq) + O2(g) + H+(aq)
उत्तर









प्रश्न 20.
निम्नलिखित अभिक्रिया से आप कौन-सी सूचनाएँ प्राप्त कर सकते हैं-
(CN)2(g) + 2OH– (aq) → CN– (aq) + CNO– (aq) + H2O(l)
उत्तर
यह एक असमानुपातन (disproportionation) अभिक्रिया है। इसमें (CN)2 एक ही समय में CN– में अपचयित और CNO– में ऑक्सीकृत होता है। यह अभिक्रिया क्षारीय माध्यम में होती है।
प्रश्न 21.
Mn3+ आयन विलयन में अस्थायी होता है तथा असमानुपातन द्वारा Mn2+, MnO2 और H+ आयन देता है। इस अभिक्रिया के लिए सन्तुलित आयनिक समीकरण लिखिए।
उत्तर



प्रश्न 22.
Cs, Ne, I तथा F में ऐसे तत्व की पहचान कीजिए, जो
(क) केवल ऋणात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ख) केवल धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ग) ऋणात्मक तथा धनात्मक दोनों ऑक्सीकरण अवस्था प्रदर्शित करता है।
(घ) न ऋणात्मक और न ही धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
उत्तर
(क) F : यह सर्वाधिक वैद्युत ऋणात्मक तत्त्व है और सदैव -1 ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ख) Cs : यह एक क्षार धातु है जो अत्यधिक वैद्युत धनात्मक है। यह सदैव +1 ऑक्सीकरण अवस्था प्रदर्शित करता है।
(ग) I: यह एक हैलोजन है। इसके संयोजक कोश में सात इलेक्ट्रॉन पाये जाते हैं। इसलिये यह -1 ऑक्सीकरण अवस्था प्रदर्शित करता है। 4-कोश (orbitals) की उपस्थिति के कारण यह +1, +3, +5, और +7 ऑक्सीकरण अवस्थाएँ भी प्रदर्शित करता है।
(घ) Ne: यह एक उत्कृष्ट गैस (noble gas) है तथा किसी रासायनिक अभिक्रिया में भाग नहीं लेती है। इसलिए, यह न तो धनात्मक ऑक्सीकरण-अवस्था में पाई जाती है और न ही ऋणात्मक ऑक्सीकरण अवस्था में।
प्रश्न 23.
जल के शुद्धिकरण में क्लोरीन को प्रयोग में लाया जाता है। क्लोरीन की अधिकता हानिकारक होती है। सल्फर डाइऑक्साइड से अभिक्रिया करके इस अधिकता को दूर किया जाता है। जल में होने वाले इस अपचयोपचय परिवर्तन के लिए सन्तुलित समीकरण लिखिए।
उत्तर
क्लोरीन तथा सल्फर डाइऑक्साइड की अभिक्रिया निम्नलिखित समीकरण द्वारा व्यक्त की जा सकती है
Cl2 + SO2 → Cl– + SO2-4
इस अपचयोपचय अभिक्रिया को आयन-इलेक्ट्रॉन विधि से निम्नांकित पदों में सन्तुलित करते हैं-
पद 1. पहले ढाँचा समीकरण लिखते हैं-
Cl2 + SO2 → Cl–+ SO2-4
पद 2. दो अर्द्ध-अभिक्रियाएँ निम्नवत् हैं-
- ऑक्सीकरण अर्द्ध-अभिक्रिया : SO2 → SO2-4
- अपचयन अर्द्ध-अभिक्रिया : Cl2 → Cl–
पद 3. ऑक्सीकरण अर्द्ध-अभिक्रिया में 0 परमाणुओं को सन्तुलित करने के लिए समीकरण में बाईं ओर दो जल अणु जोड़ते हैं-
SO2 + 2H2O → SO2-4 +4H+
पद 4. सन्तुलित अपचयन अर्द्ध-अभिक्रिया निम्नवत् होगी ।-
Cl2 → 2Cl–
पद 5. इस पद में हम दोनों अर्द्ध-अभिक्रियाओं में आवेश का सन्तुलन इस प्रकार करेंगे-
SO2 + 2H2O → SO2-4 +4H+ +2e–
Cl2 +2e– → 2Cl–
पद 6. उपर्युक्त दोनों अर्द्ध-अभिक्रियाओं को जोड़ने पर-
Cl2 + SO2 + 2H2O → 2Cl– + SO2-4 +4H+
अन्तिम सत्यापन दर्शाता है कि समीकरण परमाणुओं की संख्या एवं आवेश की दृष्टि से सन्तुलित है।
प्रश्न 24.
आवर्त सारणी की सहायता से निम्नलिखित प्रश्नों के उत्तर दीजिए-
(क) सम्भावित अधातुओं के नाम बताइए, जो असमानुपातन की अभिक्रिया प्रदर्शित कर सकती हों।
(ख) किन्हीं तीन धातुओं के नाम बताइए, जो असमानुपातन अभिक्रिया प्रदर्शित कर सकती हों।
उत्तर
(क) P4, Cl2 और S हैं।
(ख) Cu, Ga और In| इनकी असमानुपातन की अभिक्रियाएँ निम्न हैं-
2Cu+ (aq) -→ Cu2+(aq) + Cu (s)
3Ga+ (aq) → Ga3+(aq) + 2Ga(s)
3In+ (aq) → In3+(aq) + 2In (3)
ये धातु तीन ऑक्सीकरण अवस्थाओं में पायी जाती हैं, जो निम्न हैं-
Cu: +2, 0, +1
Ga : +3, 0, +1
In : +3, 0, +1
प्रश्न 25.
नाइट्रिक अम्ल निर्माण की ओस्टवाल्ड विधि के प्रथम पद में अमोनिया गैस के ऑक्सीजन गैस द्वारा ऑक्सीकरण से नाइट्रिक ऑक्साइड गैस तथा जलवाष्प बनती है। 10.0 ग्राम अमोनिया तथा 20.00 ग्राम ऑक्सीजन द्वारा नाइट्रिक ऑक्साइड की कितनी अधिकतम मात्रा प्राप्त हो सकती है?
उत्तर
प्रक्रम की रासायनिक समीकरण निम्न है-
![]()
समीकरण के अनुसार 68 ग्राम NH3 के ऑक्सीकरण के लिए 160 ग्राम O2 की आवश्यकता होती है।
∴ 10 ग्राम NH3 के ऑक्सीकरण के लिए होगी [latex]\frac { 160 }{ 68 } \times 10=23.53g[/latex] O2 की आवश्यकता। प्रक्रम में केवल 20g O2 का प्रयोग किया गया है। अत: O2 सीमान्त अभिकर्मक है।
∵ 160g O2 से प्राप्त होती है, NO= 120g
∴ 20g O2 से प्राप्त होगी, NO=[latex]\frac { 120 }{ 160 } \times 20=15.00g[/latex]
प्रश्न 26.
पाठ्य-पुस्तक की सारणी 8:1 में दिए गए मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया सम्भव है?
(क) Fe3+ तथाI(aq)
(ख) Ag+ तथा Cu(s)
(ग) Fe3+(aq) तथा Br (aq)
(घ) Ag(s) तथा Fe3+(aq)
(ङ) Br2(aq) तथा Fe2+
उत्तर
(क) सम्भव है- 2Fe3+(aq) + 2I– (aq) → 2Fe2+ (aq) + I2(s)
(ख) सम्भव है- Cu (s) + 2Ag+ (aq) Cu2+ (aq) + 2Ag (s)
(ग) सम्भव है- Cu (s) + 2Fe3+(aq) → Cu2+ (aq) + 2Fe2+ (aq)
(घ) सम्भव नहीं है।
(ङ) सम्भव है— Br2 (aq) +2Fe2+(aq) 2Br– (aq) + 2Fe3+(aq)
प्रश्न 27.
निम्नलिखित में से प्रत्येक के विद्युत-अपघटन से प्राप्त उत्पादों के नाम बताइए-
(क) सिल्वर इलेक्ट्रोड के साथ AgNO का जलीय विलयन
(ख) प्लैटिनम इलेक्ट्रोड के साथ AgNO का जलीय विलयन
(ग) प्लैटिनम इलेक्ट्रोड के साथ H,SO4 का तनु विलयन ।
(घ) प्लैटिनम इलेक्ट्रोड के साथ CuCl2 का जलीय विलयन।
उत्तर
(क) कैथोड पर Ag प्राप्त होती है। ऐनोड घुलकर Ag+ आयन देगा।
(ख) कैथोड पर Ag, ऐनोड पर O2।
(ग) कैथोड पर H2, ऐनोड पर O2
(घ) कैथोड पर Cu, यदि विलयन सान्द्र है तो ऐनोड पर Cl2 अन्यथा O2।
प्रश्न 28.
निम्नलिखित धातुओं को उनके लवणों के विलयन में से विस्थापन की क्षमता के क्रम में लिखिए-
Al, Cu, Fe, Mg तथा Zn
उत्तर
Mg > Al> Zn > Fe>Cu
प्रश्न 29.
नीचे दिए गए मानक इलेक्ट्रोड विभवों के आधार पर धातुओं को उनकी बढ़ती अपचायक क्षमता के क्रम में लिखिए-
K+/K= -2.93V, Ag+/Ag= 0.80 V, Hg2+/Hg= 0.79V
Mg2+/Mg = -2.37 V, Cr3+/Cr = -0-74V
उत्तर
Ag < Hg < Cr < Mg < K
प्रश्न 30.
उस गैल्वेनी सेल कों चित्रित कीजिए, जिसमें निम्नलिखित अभिक्रिया होती है
Zn(s) +2Ag+ (aq) → Zn2+ (aq) + 2Ag(s)
अब बताइए कि-
(क) कौन-सा इलेक्ट्रोड ऋण आवेशित है?
(ख) सेल में विद्युत-धारा के वाहक कौन हैं?
(ग) प्रत्येक इलेक्ट्रोड पर होने वाली अभिक्रियाएँ क्या हैं?
उत्तर
Zn (s)|Zn2+ (aq) || Ag+ (aq)| Ag (5)
(क) Zn/ Zn2+ इलेक्ट्रोड ऋण आवेशित है।
(ख) बाह्य परिपथ में वैद्युत धारा के वाहक इलेक्ट्रॉन हैं जिनका प्रवाह Zn इलेक्ट्रोड से Ag इलेक्ट्रोड की ओर होता है।
(ग) ऐनोड पर : Zn (s) → Zn2+ (aq) +2e–
कैथोड पर : 2Ag+ (aq) + 2e– → 2Ag (s)
परीक्षोपयोगी प्रश्नोत्तर
बहुविकल्पीय प्रश्न
प्रश्न 1.
CHC2 में कार्बन की ऑक्सीकरण संख्या है
(i) 0
(ii) + 2
(iii) -2
(iv) +4
उत्तर
(ii) +2
प्रश्न 2.
NaOCl तथा NaClO3 में क्लोरीन की ऑक्सीकरण संख्या है-
(i) + 1, +2
(ii) +1, +5
(iii) -1, +5
(iv) -1,-5
उत्तर
(ii) +1, +5
प्रश्न 3.
OF2 एवं H2O2 में ऑक्सीजन की ऑक्सीकरण संख्या है
(i) – 2,- 1
(ii) + 2, – 1
(iii) + 2, + 1
(iv) – 2,+ 1
उत्तर
(ii) +2,-1
प्रश्न 4.
S4O2-6 एवं S2O2-8 में S की ऑक्सीकरण संख्या है-
(i) + 2.5,+ 6
(ii) + 2.5,+7
(iii) – 2.5, + 6
(iv) + 2.5,- 6
उत्तर
(ii) + 2.5,+ 7
प्रश्न 5.
CH2O में कार्बन की ऑक्सीकरण संख्या है-
(i) -2
(ii) +2
(iii) 0
(iv) +4
उत्तर
(iii) 0
प्रश्न 6.
CH2Cl2 में कार्बन की ऑक्सीकरण संख्या है-
(i) +2
(ii) +1
(iii) 0
(iv) +4
उत्तर
(iii) 0
प्रश्न 7.
H2S2O8 में s की ऑक्सीकरण संख्या है-
(i) +4
(ii) +5
(iii) +6
(iv) +7
उत्तर
(iii) +6
प्रश्न 8.
ऑक्सीजन की सर्वाधिक ऑक्सीकरण संख्या प्रदर्शित करने वाला यौगिक है
(i) H2O2
(ii) F2O
(iii) Cl2O2-7
(iv) NaOCl
उत्तर
(ii) F2O
प्रश्न 9.
H2SO4, H2SO4 तथा SO2Cl2 में s की ऑक्सीकरण संख्याएँ क्रमशः हैं-
(i) +6, +4, +6
(ii) +6, +6, +4
(iii) +6, -6 +4
(iv) -4, +6, +6
उत्तर
(i) +6, +4, +6
प्रश्न 10.
निम्नलिखित यौगिकों में से किसमें Mn की ऑक्सीकरण संख्या अधिकतम है?-
(i) Mn2O3
(ii) KMnO4
(iii) K2MnO4
(iv) MnO2
उत्तर
(ii) KMnO4
प्रश्न 11.
Mn की ऑक्सीकरण संख्या K2MnO4 तो MSO4 में क्रमशः है-
(i) +7 और 12
(ii) +6 और +2
(iii) + 5 और +2
(iv) +2 और +6
उत्तर
(ii) +6 और +2
प्रश्न 12.
पोटैशियम डाइक्रोमेट में क्रोमियम की ऑपलीकरण संख्या है-
(i) +2
(ii) + 3
(iii) +4
(iv) +6
उत्तर
(iv) + 6
प्रश्न 13.
निम्नलिखित में से किसमें नाइट्रोजन की औसीकरण संख्या भिन्नात्मक है?
(i) N2H4
(ii) Ca3N2
(iii) HN3
(iv) N2F2
उत्तर
(ii) HN3
प्रश्न 14.
एक अभिक्रिया में एक धातु आयन M2+ से दो इलेक्ट्रॉनों के निष्कासित होने के बाद ऑक्सीकरण संख्या हो जाती है-
(i) शून्य
(ii) +2
(iii) +1
(iv) +4
उत्तर
(iv) +4
प्रश्न 15.
क्लोरीन की सर्वाधिक ऑक्सीकरण संख्या प्रदर्शित करने वाला यौगिक है–
(i) ClO2
(ii) Cl2O
(iii) Cl2O7
(iv) NaClO3
उत्तर
(iii) Cl2O7
प्रश्न 16.
Sg, S2F2 और H2S में सल्फर की ऑक्सीकरण संख्या के मान क्रमशः हैं|
(i) + 2, + 1 तथा -2
(ii) -2,-1 तथा + 2
(iii) 0, + 1 तथा + 2
(iv) 0, + 1 तथा – 2
उत्तर
(iv) 0, + 1 तथा – 2
प्रश्न 17.
Cl2 NaOCl तथा ClO–3 में Cl की क्रमशः ऑक्सीकरण संख्याओं के मान हैं-
(i) +2, 0, +5
(ii) 0, + 2, +5
(iii) +2, +, +5
(iv) 0, + 1, +5
उत्तर
(iv) 0, +1, +5
प्रश्न 18.
Na2S4O6 की ऑक्सीकरण संख्या है-
(i) + 2
(ii) + 3
(iii) + 15
(iv) + 2.5
उत्तर
(iv) + 2.5
प्रश्न 19.
Ni(CO)4 में Ni की ऑक्सीकरण संख्या है-
(i) 0
(ii) 4
(iii) 8
(iv) 2
उत्तर
(i) 0
प्रश्न 20.
सोडियम नाइट्रोपुसाइड में आयरन (Fe) की ऑक्सीकरण संख्या है-
(i) +3
(ii) +2
(iii) +4
(iv) 0
उत्तर
(ii) +2
प्रश्न 21.
निम्नलिखित में Mn की न्यूनतम ऑक्सीकरण संख्या वाला यौगिक है-
(i) KMnO4
(ii) MnO2
(iii) KaMnO4
(iv) Mn2O3
उत्तर
(iv) Mn2O3
प्रश्न 22.
O3 तथा H2O2में ऑक्सीजन की ऑक्सीकरण संख्या के मान क्रमशः हैं-
(i) 0, -1
(ii) 0, +1
(iii) 0-2
(iv) -2,-1
उत्तर
(i) 0, -1
प्रश्न 23.
निम्न में कौन-सी रेडॉक्स अभिक्रिया है?
(i) AgNO3 + HCl → AgCl + HNO3
(ii) BaO2 + H2SO4 → BaSO4 + H2O2
(iii) SO2 + 2H2S → 2H2O+ 3s
(iv) CaC2O4 +2HCl → CaCl2 + H2C2O4
उत्तर
(iii) SO2 + 2H2S→ 2H2O+ 3s
प्रश्न 24.
निम्नलिखित अभिक्रिया में ऑक्सीकारक है-
2CrO2-2 + 2H+ → Cr2O2-7 + H2O
(i) H+
(ii) CrO2-4
(iii) Cr+3
(iv) इनमें से कोई नहीं
उत्तर
(iv) इनमें से कोई नहीं
प्रश्न 25.
निम्न अभिक्रिया में अपचयित होने वाला पदार्थ है–
2CusO4+ 4KI→ Cu2I2 + 2K2SO4+I2
(i) CuSO4
(ii) KI
(iii) Cu2I2
(iv) I2
उत्तर
(i) CuSO4
प्रश्न 26.
हाइड्रोजन द्वारा अपचयित होने वाला ऑक्साइड है
(i) MnO2
(ii) MgO
(iii) CaO
(iv) CoO
उत्तर
(iv) CoO
प्रश्न 27.
4Fe + 3O2 → 4Fe3+ + 6O2- अभिक्रिया में निम्न में कौन-सा कथन सही नहीं है?
(i) रेडॉक्स अभिक्रिया है।
(ii) Fe अपचायक है।
(iii) Fe का अपचयन Fe3+ में हुआ है।
(iv) ऑक्सीजन का अपचयन हुआ है।
उत्तर
(iii) Fe का अपचयन Fe3+ में हुआ है।
प्रश्न 28.
298 K पर अर्द्ध अभिक्रियाओं के मानक अपचयन विभव हैं
(i) zn2+ +2e– → Zn (s); – 0.762
(ii) Cr3++ 3e– → Cr (3);- 0.740
(iii) 2H+ +2e– → H2 (g);- 0.000
(iv) Fe3+ + e– → Fe3+(aq); + 0.770
कौन-सा प्रबलतम अपचायक है।
(i) Zn (s)
(ii) Cr (s)
(iii) H2 (g)
(iv) Fe2+ (aq)
उत्तर
(i) Zn (s)
अतिलघु उत्तरीय प्रश्न
प्रश्न 1.
रेडॉक्स अभिक्रिया की व्याख्या एक उदाहरण सहित कीजिए।
उत्तर
परमाणु या आयन जिस अभिक्रिया में इलेक्ट्रॉन त्यागता है, उसे ऑक्सीकरण और जिसमें इलेक्ट्रॉन ग्रहण करता है, उसे अपचयन कहते हैं। ऑक्सीकरण तथा अपचयन क्रियाएँ साथ-साथ चलती हैं क्योंकि जब कोई परमाणु या आयन एक इलेक्ट्रॉन त्यागेगा तो उसको ग्रहण करने वाला कोई अन्य परमाणु या आयन ही होगा अर्थात् जब किसी अभिक्रिया में एक पदार्थ का ऑक्सीकरण होता है। तो दूसरे किसी अन्य पदार्थ का अपचयन भी होता है। स्पष्ट है कि ऑक्सीकरण व अपचयन क्रियाएँ साथ-साथ होती हैं। इन ऑक्सीकरण व अपचयन अभिक्रियाओं को सम्मिलित रूप से ऑक्सीकरण-अपचयन अभिक्रिया या रेडॉक्स अभिक्रिया कहते हैं।
उदाहरणार्थ-
2HgCl2 + SnCl2 → Hg2Cl2 + SnCl4
उपर्युक्त अभिक्रिया में HgCl2 का Hg2Cl2 में अपचयन होता है और HgCl2, SnCl2 को SnCl4 में ऑक्सीकृत कर देता है।
प्रश्न 2.
ऑक्सीकरण संख्या के आधार पर ऑक्सीकारक तथा अपचायक की पहचान किस प्रकार की जाती है? एक उदाहरण से स्पष्ट कीजिए।
उत्तर
ऑक्सीकरण संख्या के आधार पर, ऑक्सीकारक वह पदार्थ है जिसकी ऑक्सीकरण संख्या घटती है, जबकि अपचायक पदार्थ की ऑक्सीकरण संख्या बढ़ती है। उदाहरणार्थ-ऑ०सं. प्रति परमणु लिखने पर,

उपर्युक्त अभिक्रिया में SnCl2 में Sn की ऑक्सीकरण संख्या +2 है तथा उत्पाद SnCl4 में +4 है। Sn की ऑक्सीकरण संख्या में वृद्धि हो रही है।
∴ SnCl2 अपचायक है जबकि FeCl3 में Fe की ऑक्सीकरण संख्या +3 व FeCl2 में Fe की ऑक्सीकरण संख्या +2 है, अत: FeCl3 ऑक्सीकारक है।
प्रश्न 3.
निम्नलिखित अभिक्रिया की दो अर्द्ध अभिक्रियाएँ लिखिए। यह भी उल्लेख कीजिए कि कौन-सी अर्द्ध अभिक्रिया ऑक्सीकरण व कौन-सी अपचयन अभिक्रिया है?
SnCl2 + 2HgCl2 → SnCl4 + Hg2Cl2
उत्तर
प्रश्न में उल्लिखित अभिक्रिया को दो अर्द्ध अभिक्रियाओं में निम्नलिखित प्रकार से व्यक्त कर सकते हैं-
- SnCl2 + Cl2 → SnCl2 (ऑक्सीकरण अभिक्रिया)
- 2HgCl2 → Hg2Cl2 + Cl2 ↑ (अपचयन अभिक्रिया)
इस अभिक्रिया में HgCl2 में Hg की ऑक्सीकरण संख्या +2 है तथा Hg2Cl2 में Hg की ऑक्सीकरण संख्या 0 है। चूंकि ऑक्सीकरण संख्या में कमी हो रही है, अतः Hg2Cl2 ऑक्सीकारक है|
प्रश्न 4.
कारण सहित बताइए कि निम्नलिखित अभिक्रिया में कौन ऑक्सीकारक तथा कौन अपचायक है?
2KI + Cl2 → 2KCI + I2
उत्तर
![]()
चूंकि KI में 1 की ऑक्सीकरण संख्या -1 तथा I2 में 0 है, अर्थात् I की ऑक्सीकरण संख्या में वृद्धि हो रही है, अतः KI अपचायक है। इसके विपरीत, Cl2 में CI की ऑक्सीकरण संख्या 0 है तथा KCI में -1 है। चूंकि ऑक्सीकरण संख्या में कमी हो रही है, अतः Cl2 ऑक्सीकारक है।
प्रश्न-5.
ऑक्सीकरण संख्या को उदाहरण सहित समझाइए।
या
ऑक्सीकरण संख्या पर टिप्पणी लिखिए।
उत्तर
किसी यौगिक या आयन में तत्त्व के एक परमाणु पर स्थित धन या ऋण आवेशों की संख्या उस तत्त्व की ऑक्सीकरण संख्या कहलाती है, जबकि उस अणु या आयन में उपस्थित अन्य परमाणुओं को उनके सम्भावित आयनों के रूप में पृथक् कर दिया जाता है। यह संख्या धनात्मक व ऋणात्मक दोनों प्रकार की हो सकती है। उदाहरणार्थ-NaCl में Na की ऑक्सीकरण संख्या +1 और Cl की ऑक्सीकरण संख्या -1 है, क्योंकि Na पर इकाई धनावेश तथा Cl पर इकाई ऋणावेश है।
प्रश्न 6.
शून्य, -1 तथा +1 ऑक्सीकरण संख्या से क्या तात्पर्य है?
उत्तर
एक यौगिक में किसी तत्त्व की ऑक्सीकरण संख्या शून्य (0) से तात्पर्य है कि तत्त्व के परमाणु पर धन या ऋण आवेश नहीं है अर्थात् परमाणु विद्युत उदासीन है। तत्त्व की ऑक्सीकरण संख्या +1 से तात्पर्य यह है कि तत्त्व के परमाणु पर इकाई धन आवेश है, जिसे उदासीन करने के लिए एक इलेक्ट्रॉन ग्रहण करने की आवश्यकता होती है। तत्त्व की ऑक्सीकरण संख्या -1 से तात्पर्य है कि तत्त्व के ” परमाणु पर इकाई ऋणावेश है, जिसे उदासीन करने के लिए एक इलेक्ट्रॉन त्यागने की आवश्यकता होती है।
प्रश्न 7.
ब्लू परक्रोमेट में Cr की ऑ०सं० ज्ञात कीजिए।
उत्तर
ब्लू परक्रोमेट की संरचना

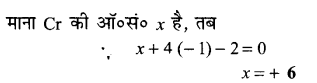
प्रश्न 8.
सम्बन्धित तत्त्वों की ऑक्सीकरण संख्या ज्ञात कीजिए
(i) KMnO4 में Mn की
(ii) ClO–3में Cl की
(iii) NaOCl में Cr की
(iv) H2S2O6 में S की
(v) Cl2 में Cl की
उत्तर

प्रश्न 9.
निम्नलिखित यौगिकों में s (सल्फर) की ऑक्सीकरण संख्या बताइए-
(i) Na2S4O6,
(ii) SO2Cl2
उत्तर
(i) Na2S4O6-माना S की ऑक्सीकरण संख्या x है। अत:

(ii) SO2Cl2-माना S की ऑक्सीकरण संख्या x है। अत:

प्रश्न 10.
K2FeO4 में Fe तथा NH–4 में N की ऑक्सीकरण संख्या ज्ञात कीजिए।
उत्तर

प्रश्न 11.
I—Cl में ci तथा H—H में H की ऑक्सीकरण संख्या ज्ञात कीजिए। कारण भी दीजिए।
उत्तर
I—Cl में Cl की ऑक्सीकरण संख्या -1 होगी; क्योंकि Cl की विद्युत ऋणात्मकता I से अधिक है, जबकि H—H में H की ऑक्सीकरण संख्या शून्य होगी क्योंकि समान परमाणु वाले यौगिक के अणुओं में तत्त्वों के परमाणु की ऑक्सीकरण संख्या शून्य होती है।
प्रश्न 12.
S8 अणु में s की संयोजकता तथा ऑक्सीकरण संख्या क्या है?
उत्तर
S8 में S की संयोजकता 2 है, जबकि ऑक्सीकरण संख्या शून्य है।
प्रश्न 13.
निम्नलिखित समीकरण को सन्तुलित एवं पूर्ण कीजिए-
SO2+ MnO–4+…… → SO2-4 + Mn2+ +…..
उत्तर

प्रश्न 14.
आयनिक समीकरण Br2 + OH– → Br– + BrO–3 + H2O को सन्तुलित कीजिए तथा ऑक्सीकारक और अपचायक बताइए।
उत्तर
दी गई आयनिक अभिक्रिया समीकरण को अर्द्ध अभिक्रिया समीकरण के रूप में लिखने पर,
Br2 → Br– …(i)
Br2 → BrO–3 …(ii)
समी० (i) से,
[Br2 +2e → 2Br–]x 5

प्रश्न 15.
(i) Cl2O7 में Cl की ऑक्सीकरण संख्या की गणना कीजिए।
(ii) 2FeCl3 + H2S → 2FeCl2 + 2HCI+S इस अभिक्रिया में ऑक्सीकारक और
अपचायक का नाम लिखिए।
उत्तर

प्रश्न 16.
निम्न में से किसमें Mn की ऑक्सीकरण संख्या सबसे अधिक है और क्यों?
Mn2O3, MnO2, Mno, K2MnO4
उत्तर
K2MnO4 में Mn की ऑक्सीकरण संख्या सबसे अधिक (+6) है, क्योंकि इसमें ऑक्सीजन परमाणुओं का आपेक्षिक अनुपात बाकी अणुओं से अधिक है।
प्रश्न 17.
निम्नलिखित समीकरण को सन्तुलित कीजिए।
Fe2+ + NO–3 + H+ —> Fe2 + …. + H2O
उत्तर

प्रश्न 18.
विद्युत रासायनिक श्रेणी के आधार पर F, CI, Br तथा I की ऑक्सीकारक क्षमता को समझाइए।
या
कारण देते हुए समझाइए कि हैलोजन ऑक्सीकारक के रूप में क्यों कार्य करते हैं?
उत्तर
हैलोजनों की ऑक्सीकारक क्षमता उनके इलेक्ट्रॉन ग्रहण करने की प्रवृत्ति पर निर्भर करती है। जिस हैलोजन की इलेक्ट्रॉन ग्रहण करने की प्रवृत्ति अधिक होती है वह अधिक प्रबल ऑक्सीकारक होता है। अधिक प्रबल ऑक्सीकारक के रेडॉक्स युग्म का मानक अपचयन विभव अधिक धनात्मक होता है। हैलोजनों (X2) की ऑक्सीकारक क्षमता उनके रेडॉक्स युग्मों (X2/X–) के मानक अपचयन विभवों के मान बढ़ने के क्रम में बढ़ती है।

लघु उत्तरीय प्रश्न
प्रश्न 1.
इलेक्ट्रॉनिक सिद्धान्त के आधार पर ऑक्सीकरण-अपचयन अभिक्रिया को उदाहरण देकर समझाइए।
उत्तर
ऑक्सीकरण—किसी परमाणु, अणु या आयन के इलेक्ट्रॉनों का पृथक् होना ऑक्सीकरण कहलाता है। इसके फलस्वरूप धनात्मक संयोजकता बढ़ती है तथा ऋणात्मक संयोजकता घटती है जो कि त्यागे गये इलेक्ट्रॉन संख्या के बराबर होती है। चूंकि इस क्रिया में इलेक्ट्रॉन त्यागे जाते हैं अत: इसे इलेक्ट्रॉन वियोजन भी कहते हैं।
उदाहरणार्थ–
(i) Fe2+ → Fe3+ +e– (धनात्मक संयोजकता का बढ़ना)
(ii) 2Cl– → Cl2 + 2e– (ऋणात्मक संयोजकता का घटना)
अपचयन-किसी परमाणु, अणु या आयन से इलेक्ट्रॉनों का जुड़ना अपचयन कहलाता है। इसके फलस्वरूप धनात्मक संयोजकता घटती है तथा ऋणात्मक संयोजकता बढ़ती है जो कि ग्रहण किये गये इलेक्ट्रॉन संख्या के बराबर होती है। चूंकि इस विभव में इलेक्ट्रॉन ग्रहण किये जाते हैं अतः इसे इलेक्ट्रॉनीकरण भी कहते हैं।
उदाहरणार्थ- (i) Fe3+ + e– → Fe2+ (धनात्मक संयोजकता का घटना)
(iii) Cl2 +2e– → 2Cl– (ऋणात्मक संयोजकता का बढ़ना)
प्रश्न 2.
ऑक्सीकरण संख्या तथा संयोजकता में क्या अन्तर है? उदाहरण देकर समझाइए।
उत्तर
- किसी तत्त्व की संयोजकता उसके एक परमाणु द्वारा स्थानान्तरित या साझे में प्रयुक्त इलेक्ट्रॉनों की संख्या को कहते हैं, जबकि किसी तत्त्व की ऑक्सीकरण संख्या उसे तत्त्व के किसी यौगिक में उसके एक परमाणु पर उपस्थित आवेश को कहते हैं।
- किसी तत्त्व की संयोजकता सदैव पूर्णाक होती है, जबकि किसी तत्त्व की ऑक्सीकरण संख्या भिन्नात्मक भी हो सकती है।
प्रश्न 3.
निम्नलिखित समीकरण को ऑक्सीकरण संख्या के आधार पर सन्तुलित कीजिए। सूत्रों के ऊपर सम्बन्धित तत्त्व की ऑक्सीकरण संख्या प्रदर्शित है।
![]()
उत्तर
इस अभिक्रिया में कॉपर और नाइट्रोजन की ऑक्सीकरण संख्या में परिवर्तन हुआ है।
कॉपर की ऑक्सीकरण संख्या में वृद्धि = 2 यूनिट प्रति परमाणु Cu
नाइट्रोजन की ऑक्सीकरण संख्या में कमी = 1 यूनिट प्रति अणु HNO3 सन्तुलित समीकरण में ऑक्सीकरण संख्या में हुई कुल वृद्धि और कुल कमी दोनों का बराबर होना
आवश्यक है, अत: समीकरण में HNO3 को 2 से तथा Cu को 1 से गुणा करना आवश्यक है। ऐसा करने पर निम्नलिखित समीकरण प्राप्त होती है
Cu+2HNO3 →Cu(NO3)2 + 2NO2 + H2O
Cu(NO3)2 में एक कॉपर परमाणु से दो नाइट्रेट मूलक संयुक्त हैं, अत: समीकरण को सन्तुलित करने के लिए HNO3 के दो और अणुओं की आवश्यकता पड़ेगी तथा हाइड्रोजन और ऑक्सीजन परमाणुओं की संख्या सन्तुलित करने के लिए H2O अणु को 2 से गुणा करना आवश्यक है।
Cu+4HNO3 →Cu(NO3)2 + 2NO2 + 2H2O यह समीकरण सन्तुलित है।
प्रश्न 4.
निम्नलिखित अभिक्रिया को ऑक्सीकरण अंक विधि द्वारा पूर्ण एवं संतुलित कीजिए
I2 + HNO3 → NO2 + HIO3
उत्तर

प्रश्न 5.
निम्नलिखित अभिक्रिया को सन्तुलित कीजिए-
Zn + HNO3 → Zn(NO3)2 + NO2 + H2O
उत्तर

प्रश्न 6.
आयन-इलेक्ट्रॉन विधि द्वारा अम्लीय माध्यम में निम्न अभिक्रिया की समीकरण सन्तुलित कीजिए
MnO–4 + Fe2+ → Fe3+ + Mn2+ + H2O
उत्तर
सर्वप्रथम समीकरण के ऑक्सीकारकों तथा अपचायकों की अर्द्ध-अभिक्रियाएँ पृथक्-पृथक् सन्तुलित की जाती हैं; जैसे-
प्रथम अर्द्ध-अभिक्रिया।
MnO–4 → Mn2- (अपचयन)
ऑक्सीजन सन्तुलित करने के लिए 4H2O दाईं तरफ जोड़े जाते हैं। अतः
MnO–4 → Mn2+ +4H2O
फिर हाइड्रोजन सन्तुलित करने के लिए 8H+ बाईं तरफ जोड़े जाते हैं। अत:
MnO–4 + 8H+ → Mn2+ +4H2O
अब समीकरण में दोनों तरफ आवेश सन्तुलित करने के लिए 5e– बाईं तरफ जोड़ने पर निम्नलिखित समीकरण मिलती है-
MnO–4 +8H+ +5e– → Mn2+ +4H2O …..(i)
दूसरी अर्द्ध-अभिक्रिया
Fe2+ → Fe3+ (ऑक्सीकरण)
आवेश सन्तुलित करने के लिए दाईं तरफ le– जोड़ने पर,
Fe2+ → Fe3+ +e– …(ii)
अब समीकरण (ii) में 5 की गुणा करके, इसे समीकरण (i) में जोड़ने पर निम्नलिखित समीकरण प्राप्त होती है-
MnO–4 + 8H+ + 5Fe2+ +5e– → 5Fe3+ + Mn2+ +4H2O+ 5e–
इस समीकरण में दोनों तरफ से 5e2 कट जाते हैं। अतः
MnO–4 + 8H+ + 5Fe2+ → 5Fe3+ + Mn2+ +4H2O
यही सन्तुलित समीकरण है।
प्रश्न 7.
निम्नलिखित रासायनिक अभिक्रिया की समीकरण को आयन-इलेक्ट्रॉन विधि से सन्तुलित कीजिए-
K2Cr2O7 + H2SO4 + FeSO4→ Fe2(SO4)3 + Cr2(SO4)3+ K2SO4 + H2O
उत्तर


विस्तृत उत्तरीय प्रश्न
प्रश्न 1.
ऑक्सीकरण संख्या को निर्धारित करने के नियम लिखिए।
उत्तर
ऑक्सीकरण संख्या को निर्धारित करने के नियम किसी यौगिक/आयन में किसी तत्त्व की ऑक्सीकरण संख्या का मान जानने के लिए कुछ नियम बनाए गए हैं। ये नियम निम्नवत् हैं-
- स्वतन्त्र अथवा तात्त्विक अवस्था में उपस्थित किसी तत्त्व के प्रत्येक परमाणु की ऑक्सीकरण संख्या सदैव शून्य होती है।
उदाहरणार्थ- He, H2, O2, Cl2, O3, P4, S8, Na, Mg तथा Al में प्रत्येक परमाणु की ऑक्सीकरण संख्या शून्य है। - किसी तत्त्व के अपररूपों की ऑक्सीकरण संख्या शून्य होती है। उदाहरणार्थ-C के अपररूप हीरा तथा ग्रेफाइट दोनों की ऑक्सीकरण संख्या शून्य होती है।
- किसी एकपरमाणुक आयन (monoatomic ion) की ऑक्सीकरण संख्या उस पर उपस्थित आवेश के बराबर होती है। उदाहरणार्थ-Na+, Mg2+, Fe3+, Cl2,O2- आयनों की ऑक्सीकरण संख्याएँ क्रमशः 1, 2, 3, -1 तथा -2 हैं।
- अधातुओं के साथ यौगिकों में हाइड्रोजन की ऑक्सीकरण संख्या +1 होती है। धात्विक हाइड्राइडों | (जैसे-NaH,MgH2, LiH, CaH2 आदि) में हाइड्रोजन की ऑक्सीकरण संख्या -1 होती है।
- अधिकांश यौगिकों में ऑक्सीजन की ऑक्सीकरण संख्या -2 होती है। परॉक्साइडों (जैसे H2O2, BaO2 आदि) में ऑक्सीजन की ऑक्सीकरण संख्या -1 होती है। सुपर ऑक्साइडों (जैसे-KO2, RbO2 आदि) में प्रत्येक ऑक्सीजन परमाणु के लिए ऑक्सीकरण संख्या -92 निर्धारित की गई है। एक अन्य अपवादस्वरूप ऑक्सीजन डाइफ्लुओराइड (OF2) तथा डाइऑक्सीजन डाइफ्लुओराइड (O2F2) जैसे यौगिकों में ऑक्सीजन की ऑक्सीकरण संख्या
क्रमशः +2 तथा +1 है। - सभी क्षार धातुओं की अनेक यौगिकों में ऑक्सीकरण संख्या +1 होती है तथा सभी क्षारीय मृदा धातुओं की ऑक्सीकरण संख्या +2 होती है। ऐलुमिनियम की उसके यौगिकों में ऑक्सीकरण संख्या सामान्यतः +3 होती है।
- सभी यौगिकों में फ्लुओरीन की ऑक्सीकरण संख्या -1 होती है। यौगिकों में क्लोरीन, ब्रोमीन तथा आयोडीन की ऑक्सीकरण संख्या साधारणत: -1 होती है, परन्तु जिन यौगिकों में ये तत्त्व ऑक्सीजन से जुड़े होते हैं उन यौगिकों में इन तत्वों की ऑक्सीकरण संख्या कोई धनात्मक संख्या होती है।
- दो अधातु परमाणुओं वाले यौगिकों में अधिक विद्युत ऋणात्मक तत्त्व के परमाणु की ऑक्सीकरण संख्या ऋणात्मक होती हैं जबकि कम विद्युत ऋणात्मक तत्त्व के परमाणु की ऑक्सीकरण संख्या धनात्मक होती है। उदाहरणार्थ-NH2 तथा NI2 में N कम विद्युत ऋणात्मक परमाणु से जुड़ा है इसीलिए इसको -3 ऑक्सीकरण संख्या दी जाती है, परन्तु जब यह NF2 में अधिक विद्युत ऋणात्मक परमाणु से जुड़ा होता है, तब इसे +3 ऑक्सीकरण संख्या दी जाती है।
- उदासीन यौगिकों में सभी परमाणुओं की ऑक्सीकरण संख्याओं का बीजीय योग शून्य होता है। उदाहरणार्थ-CH4 में सभी परमाणुओं का बीजीय योग शून्य है।
- जटिल तथा बहुपरमाणुक आयनों में, आयन के सभी परमाणुओं की ऑक्सीकरण संख्याओं का बीजीय योग आयन पर उपस्थित आवेश के बराबर होता है।
धात्विक तत्त्वों की ऑक्सीकरण संख्या धनात्मक होती है तथा अधात्विक तत्त्वों की ऑक्सीकरण संख्या धनात्मक या ऋणात्मक होती है। संक्रमण धातु तत्त्व अनेक धनात्मक ऑक्सीकरण संख्या दर्शाते। हैं। -ब्लॉक के तत्त्वों के लिए उनकी उच्चतम धनात्मक ऑक्सीकरण संख्या उनकी वर्ग संख्या के बराबर होती है। 2-ब्लॉक के तत्त्वों (उत्कृष्ट गैसों को छोड़कर) के लिए उच्चतम धनात्मक ऑक्सीकरण संख्या उनकी वर्ग संख्या में से 10 घटाकर प्राप्त की जाती है। यद्यपि p-ब्लॉक के तत्त्वों के लिए उच्चतम ऋणात्मक ऑक्सीकरण संख्या 8 में से संयोजी कोश में उपस्थित इलेक्ट्रॉनों की संख्या घटाकर प्राप्त की जा सकती है। इसका अर्थ है कि आवर्त सारणी के किसी आवर्त में उच्चतम धनात्मक ऑक्सीकरण संख्या सामान्यत: बढ़ती है। आवर्त सारणी के तीसरे आवर्त में ऑक्सीकरण संख्या +1 से +7 तक बढ़ती है।
We hope the UP Board Solutions for Class 11 Chemistry Chapter 8 Redox Reactions (अपचयोपचय अभिक्रियाएँ) help you. If you have any query regarding UP Board Solutions for Class 11 Chemistry Chapter 8 Redox Reactions (अपचयोपचय अभिक्रियाएँ), drop a comment below and we will get back to you at the earliest.